Czy rak płuca ma własnych lokatorów?
Drugoplanowa postać dramatu
Prezentowane badanie sugeruje, że agresywny guz może czasem tworzyć warunki sprzyjające obecności oportunistycznego grzyba. To kolejny krok w coraz bardziej złożonym rozumieniu nowotworu – z uwzględnieniem nie tylko zbioru nieprawidłowych komórek, ale i ich mikrośrodowiska.
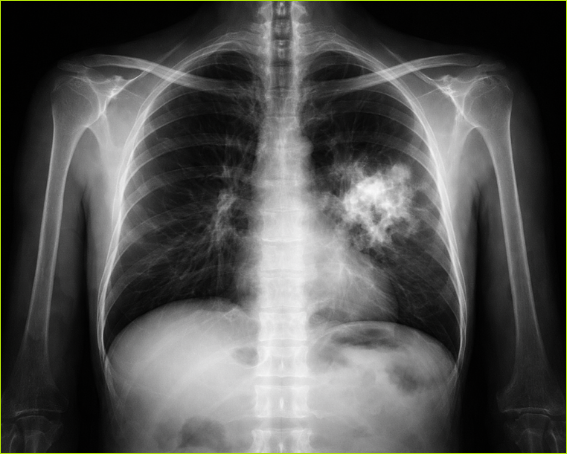
Rak płuca przez lata opisywano językiem dobrze znanym pacjentom i lekarzom – mutacje, przerzuty, tomografia komputerowa, operacja, chemia, immunoterapia. To słownik walki z jedną z najpoważniejszych chorób współczesności. Ale obok tego tradycyjnego obrazu wyrasta dziś drugi, bardziej złożony. Guz nie jest już widziany wyłącznie jako masa komórek, które wymknęły się spod kontroli. Coraz częściej przedstawia się go jako biologiczne środowisko, z naczyniami krwionośnymi, komórkami odpornościowymi, stanem zapalnym, zaburzonym metabolizmem i siecią lokalnych zależności.
Do tej układanki badacze próbują dopisać jeszcze jeden element. Mikroorganizmy.
Nowa praca zespołu z Uniwersytetu Medycznego we Wrocławiu, opublikowana w Frontiers in Cellular and Infection Microbiology, dotyczy pytania, które jeszcze kilka lat temu brzmiałoby zaskakująco – czy tkanka raka płuca może być miejscem kolonizacji przez Pneumocystis jirovecii, oportunistyczny grzyb znany przede wszystkim z ciężkich zarażeń u osób z osłabioną odpornością?
Badanie z Wrocławia
Główną autorką pracy jest dr Magdalena Szydłowicz z Katedry i Zakładu Biologii i Parazytologii Lekarskiej Wydziału Lekarskiego Uniwersytetu Medycznego we Wrocławiu. Wraz ze współpracownikami z 4. Wojskowego Szpitala Klinicznego we Wrocławiu oraz naukowcami z Czech, Hiszpanii i Francji, zespół połączył kompetencje mikrobiologiczne, kliniczne i molekularne, aby sprawdzić, czy w tkankach pobieranych od pacjentów operowanych z powodu raka płuca można wykryć DNA Pneumocystis jirovecii.
– Interesowało nas nie tyle samo wykrycie Pneumocystis, ile pytanie, czy mikrośrodowisko guza sprzyja infekcji tego patogenu. Jednocześnie możliwa jest również odwrotna zależność – obecność Pneumocystis, poprzez wywoływanie lokalnego stanu zapalnego lub innych zmian w tkance płucnej, może potencjalnie wpływać na przebieg procesów nowotworowych – mówi dr Magdalena Szydłowicz.
To badanie należy do kategorii prac eksploracyjnych. Nie testuje nowego leku. Nie porównuje dwóch metod leczenia. Nie zmienia standardów postępowania. Jego celem jest sprawdzenie, czy pewne zjawisko biologiczne w ogóle istnieje i czy warto badać je dalej. W nauce właśnie od takich pytań często zaczyna się postęp.
od lewej: dr Żaneta Zajączkowska, dr Magdalena Szydłowicz, dr hab. Marta Kicia, prof. UMW - Katedra i Zakład Biologii i Parazytologii Medycznej, Uniwersytet Medyczny we Wrocławiu
od lewej: dr Żaneta Zajączkowska, dr Magdalena Szydłowicz, dr hab. Marta Kicia, prof. UMW - Katedra i Zakład Biologii i Parazytologii Medycznej, Uniwersytet Medyczny we Wrocławiu
Czym jest Pneumocystis jirovecii?

To gatunek grzyba, który przez lata był kojarzony głównie z zapaleniem płuc u osób z głębokimi zaburzeniami odporności pacjentów z AIDS, po przeszczepieniach lub podczas intensywnego leczenia onkologicznego. W takich sytuacjach może prowadzić do ciężkiej choroby wymagającej pilnego leczenia.
Ale to tylko część obrazu.
Coraz więcej badań pokazuje, że zarażenie Pneumocystis jirovecii może również występować bez klasycznych objawów choroby, czyli w formie kolonizacji. W praktyce można to porównać do sytuacji, w której ktoś przebywa w budynku, ale niczego w nim nie niszczy. Jest obecny, lecz nie prowadzi otwartego konfliktu.
Rak jako środowisko życia

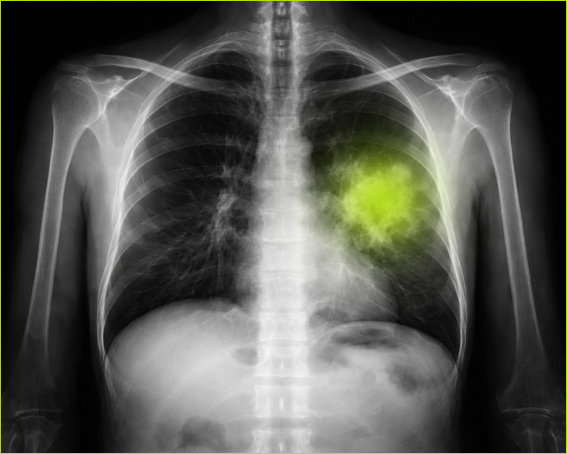
Nowotwór nie rośnie w pustce. Komórki raka wydzielają substancje chemiczne, wpływają na naczynia krwionośne, zmieniają lokalny odczyn pH, przyciągają lub wypierają komórki układu odpornościowego. Wokół guza tworzy się specyficzne mikrośrodowisko. To właśnie ono interesuje dziś onkologów równie mocno jak sam guz.
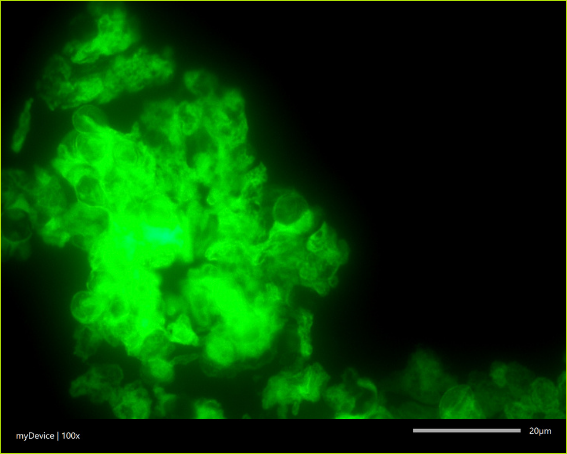
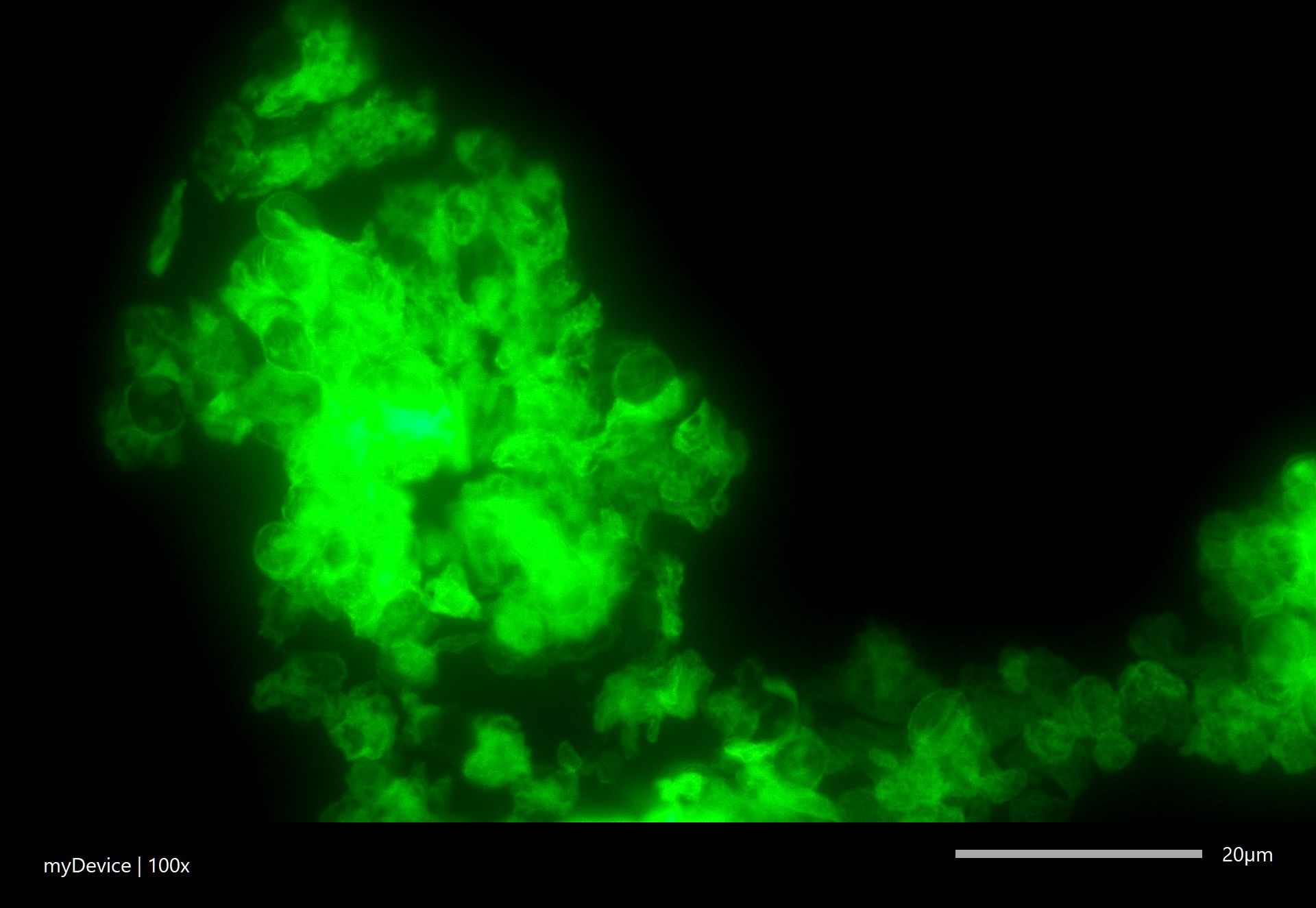
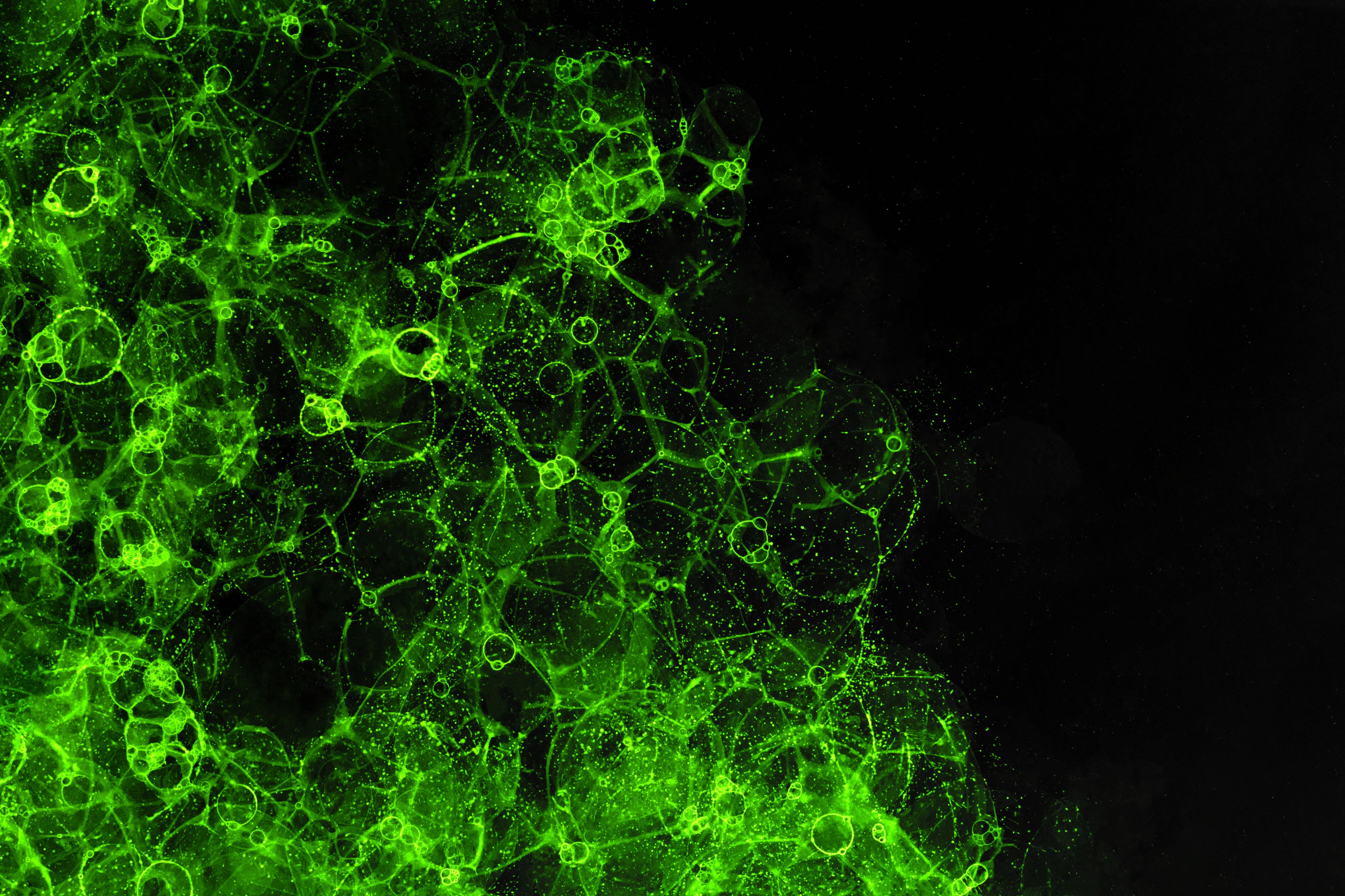
Cysty Pneumocystis jirovecii w materiale pobranym od pacjenta z pneumocystozą, znakowane metodą pośredniej immunofluorescencji.
Cysty Pneumocystis jirovecii w materiale pobranym od pacjenta z pneumocystozą, znakowane metodą pośredniej immunofluorescencji.
Bo często o przebiegu choroby decyduje nie tylko to, jakie mutacje doprowadziły do rozwoju nowotworu, lecz także to, jak wygląda jego otoczenie. Czy układ odpornościowy jest aktywny? Czy w tkance występuje przewlekły stan zapalny? Czy guz ma dobre ukrwienie? Czy reaguje na leczenie immunologiczne?
Do tego katalogu pytań zaczyna dochodzić kolejne, na które szukali odpowiedzi badacze z Wrocławia: jakie mikroorganizmy mogą się tam pojawiać?
Podcast:
Kliknij aby posłuchać!
Teatrum – ustawienie sceny

Do pracy włączono 70 pacjentów z pierwotnym rakiem płuca, operowanych między 2023 a 2025 rokiem. Istotne jest to, że byli to chorzy przed chemioterapią i bez świeżego leczenia immunosupresyjnego. Dzięki temu badacze chcieli ograniczyć wpływ terapii na wyniki.
Podczas operacji pobierano trzy rodzaje materiału: fragment tkanki nowotworowej, fragment sąsiedniej tkanki płuca, która makroskopowo nie wyglądała na zmienioną chorobowo, oraz wydzielinę z dolnych dróg oddechowych. Następnie za pomocą metody PCR poszukiwano DNA Pneumocystis jirovecii w materiale pobranym od pacjenta. Detekcja oparta na metodach molekularnych umożliwia wykrycie patogenu nawet przy niskiej intensywności zarażenia, którą charakteryzuje się kolonizacja.

Drugoplanowa postać dramatu

DNA grzyba wykryto u 8 z 70 pacjentów, czyli u około 11 procent badanych. W części przypadków materiał genetyczny obecny był w wydzielinie oddechowej lub w sąsiedniej tkance płuca. Najciekawsze było jednak to, że w samej tkance nowotworowej wykryto go tylko u dwóch osób.
Oba przypadki dotyczyły gruczolakoraka płuca o wysokim stopniu złośliwości.
– W naszych obserwacjach grzyb ten był wykrywany w tkance nowotworowej u pacjentów z bardziej zaawansowaną postacią nowotworu, co może sugerować, że takie zmienione środowisko guza sprzyja kolonizacji Pneumocystis. Trzeba jednak podkreślić, że jest to wstępna obserwacja i wymaga dalszych badań – podkreśla dr Szydłowicz.
To obserwacja interesująca, ale wymagająca dużej ostrożności. Dwa przypadki nie są podstawą do szerokich uogólnień. Mogą jednak sugerować kierunek dalszych badań. Być może bardziej agresywne nowotwory tworzą środowisko bardziej podatne na kolonizację przez niektóre mikroorganizmy.

Czego w badaniu nie wyczytamy

W erze szybkich nagłówków warto powiedzieć to jasno. Badanie nie pokazuje, że grzyb powoduje raka płuca. Nie sugeruje, że pacjenci z rakiem powinni przyjmować profilaktykę przeciwgrzybiczą. Nie dowodzi też, że obecność Pneumocystis pogarsza rokowanie.
Pokazuje jedynie, że u części chorych można wykryć materiał genetyczny tego organizmu, a w nielicznych przypadkach także w tkance guza.
Tylko dlaczego to istotne?
Współczesna medycyna rozwija się często właśnie dzięki takim drobnym przesunięciom wiedzy. Najpierw pojawia się sygnał. Potem kolejne zespoły sprawdzają go na większych grupach pacjentów. Dopiero po latach wiadomo, czy był to trop właściwy.
Dziś podobne pytania stawia się już w wielu dziedzinach onkologii. Wiadomo, że bakteria Helicobacter pylori zwiększa ryzyko raka żołądka. Wirus HPV odgrywa istotną rolę w raku szyjki macicy. W raku jelita grubego bada się znaczenie określonych bakterii jelitowych. Coraz częściej analizuje się też wpływ mikrobiomu jelit na skuteczność immunoterapii.
Pacjent na scenie

Pacjent z rakiem płuca nie powinien na podstawie tej pracy domagać się badań na Pneumocystis. Lekarz nie zmieni dziś terapii dlatego, że przeczytał artykuł naukowy dotyczący tych badań. Nie pojawiają się nowe zalecenia kliniczne. Ale znaczenie jest inne – badania te pokazują, jak zmienia się sposób myślenia o nowotworach.
Jeszcze niedawno rak był opisywany niemal wyłącznie jako problem genetyczny. Potem stał się także problemem immunologicznym. Dziś coraz częściej staje się problemem złożonym – zależnym od relacji między komórkami nowotworu, odpornością, stanem zapalnym i mikroorganizmami.
To nie zmienia leczenia jutro rano. Może jednak zmienić leczenie za kilka lat.
Autorzy sami podkreślają ograniczenia badania. Grupa pacjentów była niewielka, a dodatnich wyników w tkance guza było zaledwie dwa. To za mało, by formułować mocne wnioski.
Potrzebne są badania na szerszą skalę, najlepiej wieloośrodkowe, które sprawdzą, czy obserwacja powtarza się w innych populacjach. Ważne będzie także ustalenie, czy obecność patogenu ma wpływ na rozwój stanu zapalnego, reakcję na leczenie albo rokowanie.
– Na razie jesteśmy na etapie obserwacji, nie praktyki medycznej. Nasze wyniki mogą jednak stanowić podstawę dla przyszłych badań nad znaczeniem myko- i mikrobiomu płuc w kontekście immunologii guzów płuca oraz potencjalnych biomarkerów diagnostycznych i prognostycznych – dodaje dr Szydłowicz.

Nauka powoli odsłania scenę

Praca zespołu dr Magdaleny Szydłowicz jest właśnie taką cegiełką. Nie przełomem, nie sensacją, nie obietnicą nowej terapii. Raczej starannie postawionym pytaniem i pierwszą próbą odpowiedzi. W nauce to bardzo dużo. Bo zanim pojawi się leczenie, musi pojawić się lepsze rozumienie choroby. A ono niemal zawsze zaczyna się od tego, że ktoś odważy się zajrzeć tam, gdzie wcześniej mało kto patrzył.
D. Sikora
FAQ
1. Jaki był główny cel przeprowadzonego badania?
Głównym celem badania było ustalenie, czy nietypowy grzyb oportunistyczny, Pneumocystis jirovecii, może zasiedlać tkankę nowotworową płuc. Naukowcy chcieli sprawdzić, czy ten patogen, wykazujący tendencję do ogniskowego rozmieszczenia w płucach, gromadzi się bezpośrednio w obrębie guza.
2. Jaką grupę pacjentów objęto analizą?
W badaniu wzięło udział 70 pacjentów z histologicznie potwierdzonym pierwotnym rakiem płuca, u których nie stosowano chemioterapii ani leczenia immunosupresyjnego w ciągu sześciu miesięcy przed rozpoczęciem badań. Większość rozpoznań (ponad 91%) stanowiły raki niedrobnokomórkowe (NSCLC).
3. Jakie rodzaje próbek pobierano do badań?
Od każdego pacjenta pobierano śródoperacyjnie trzy rodzaje materiału: fragmenty tkanki nowotworowej (NPL), fragmenty tkanki przyległej (NAT) oraz wydzielinę z dróg oddechowych (RS).
4. Jak często wykrywano obecność P. jirovecii u badanych osób?
DNA grzyba wykryto u 8 z 70 pacjentów (11,4%). Łącznie patogen zidentyfikowano w 14 próbkach pochodzących od tych osób.
5. Czy potwierdzono obecność patogenu bezpośrednio w tkance nowotworowej?
Tak, DNA P. jirovecii wykryto w próbkach tkanki nowotworowej (NPL) u dwóch pacjentów. Stanowiło to 25% wszystkich osób z wynikiem dodatnim. W obu tych przypadkach patogen był obecny jednocześnie we wszystkich trzech rodzajach badanych próbek (NPL, NAT i RS).
6. Czy stopień złośliwości nowotworu ma związek z obecnością grzyba?
Badanie wykazało istotną statystycznie korelację: obecność Pneumocystis w tkance nowotworowej (NPL) była ograniczona wyłącznie do pacjentów z guzami o wysokim, trzecim stopniu złośliwości histologicznej (G3). Sugeruje to, że zaawansowane stadium nowotworu może tworzyć specyficzne mikrośrodowisko ułatwiające kolonizację.
7. Jakie metody laboratoryjne wykorzystano do wykrycia patogenu?
Zastosowano metodę nested-PCR, w której amplifikowano fragmenty genów mitochondrialnych grzyba (mtLSU rRNA oraz CYB). Następnie przeprowadzono genotypowanie poprzez analizę polimorfizmów pojedynczych nukleotydów (SNP), co pozwoliło na identyfikację konkretnych szczepów patogenu.
8. Czy pacjenci z wynikiem dodatnim wykazywali objawy zapalenia płuc?
Nie. Żaden z pacjentów nie wykazywał klinicznych ani radiologicznych objawów pneumocystozowego zapalenia płuc (PCP). W związku z tym osoby te sklasyfikowano jako skolonizowane.
9. Dlaczego kolonizacja tym grzybem jest niebezpieczna dla pacjentów onkologicznych?
Mimo braku objawów, kolonizacja jest istotna klinicznie, ponieważ może wywoływać stan zapalny i uszkodzenia tkanki płucnej. Co więcej, u pacjentów z rakiem płuca istnieje wysokie ryzyko rozwoju pełnoobjawowego zapalenia płuc (PCP) np. w wyniku osłabienia odporności spowodowanego późniejszym leczeniem onkologicznym.
10. Jakie są najważniejsze wnioski z badania dla praktyki medycznej?
Autorzy sugerują rozważenie rutynowych badań przesiewowych w tej grupie pacjentów, zwłaszcza przed rozpoczęciem leczenia onkologicznego, oraz wskazują na potencjalną rolę mikrobiomu płuc jako biomarkera w diagnostyce raka.
Powerd by NotebookLM
Materiał powstał na podstawie artykułu:
Multi-site screening for Pneumocystis jirovecii in lung cancer: possible tumour tissue colonization
DOI: 10.3389/fcimb.2026.1755638
Autorzy i autortki: Magdalena Szydłowicz, Żaneta Zajączkowska, Mariusz Chabowski, Maciej Nowicki, Błażej Łukianowski, Paweł Gajdzis, Martin Kváč, Enrique J. Calderón, Solène Le Gal, Marta Kicia
Web. A. Maj
Photos: freepik.com, archwium własne autorów